植物在逆境下或衰老时,由于体内活性氧代谢加强而使H2O2发生累积。过氧化氢酶可以清除H2O2,是植物体内重要的酶促防御系统之一。因此,植物组织中过氧化氢酶活性与植物的抗逆性密切相关,本实验利用高锰酸钾滴定法测定过氧化氢酶活性。
一、实验原理
过氧化氢酶(CAT)属于血红蛋白酶,含有铁,它能催化过氧化氢分解为水和分子氧,在此过程中起传递电子的作用,过氧化氢则既是氧化剂又是还原剂。在反应系统中加入一定量(反应过量)的H2O2溶液,经酶促反应后,用标准高锰酸钾溶液(在酸性条件下)滴定多余的H2O2,即可求出消耗的H2O2的量。
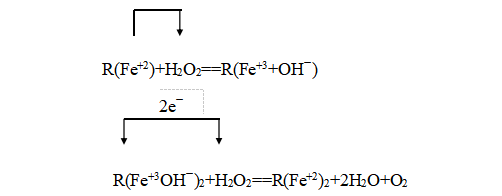
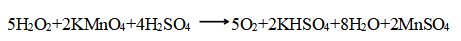
二、实验仪器
研钵、三角瓶50m、酸式滴定管(10ml)、恒温水浴、容量瓶25ml。
三、实验试剂
10% H2SO4;
0.2mol/L磷酸缓冲液pH7.8;
0.1mol/L高锰酸钾标准液:称取KMnO4(AR)3.1605g,用新煮沸冷却蒸馏水配制成1000ml,用0.1mol/L草酸溶液标定;
0.1mol/L H2O2:市售30% H2O2大约等于17.6mol/L,取30% H2O2溶液5.68ml,稀释至1000ml,用标准0.1mol/ KMnO4溶液(在酸性条件下)进行标定;
0.1mol/L草酸:称取优级纯H2C2O4·2H2O 12.607g,用蒸馏水溶解后,定容至1L。
四、测定步骤
1.酶液提取 取样品2.5g加入pH7.8的磷酸缓冲溶液少量,研磨成匀浆,转移至25ml容量瓶中,用该缓冲液冲洗研钵,并将冲洗液转入容量瓶中,用同一缓冲液定容,4000rpm离心15min,上清液即为过氧化氢酶的粗提液。
2.取50ml三角瓶4个(两个测定两个对照),测定瓶中加入酶液2.5ml,对照瓶中加入煮死酶液2.5ml,再加入2.5ml 0.1mol/L H2O2,同时计时,于30℃恒温水浴中保温10min,立即加入10% H2SO4 2.5ml。
3.用0.1mol/L KMnO4标准溶液滴定H2O2,至出现粉红色(在30min内不消失)为终点。
五、结果计算
酶活性用每克鲜重样品1min内分解H2O2的毫克数表示:
过氧化氢酶活性(mg/g·min)=(A-B)×VT÷Vs×1.7÷W÷t
式中:
A—对照KMnO4滴定毫升数;
B—酶反应后KMnO4滴定毫升数;
VT—提取酶液总量(ml);
Vs—反应所用酶液量(ml);
W—样品鲜重(g);
t—反应时间(min);
1.7—1ml 0.1mol/L的KMnO4相当于1.7mg H2O2。